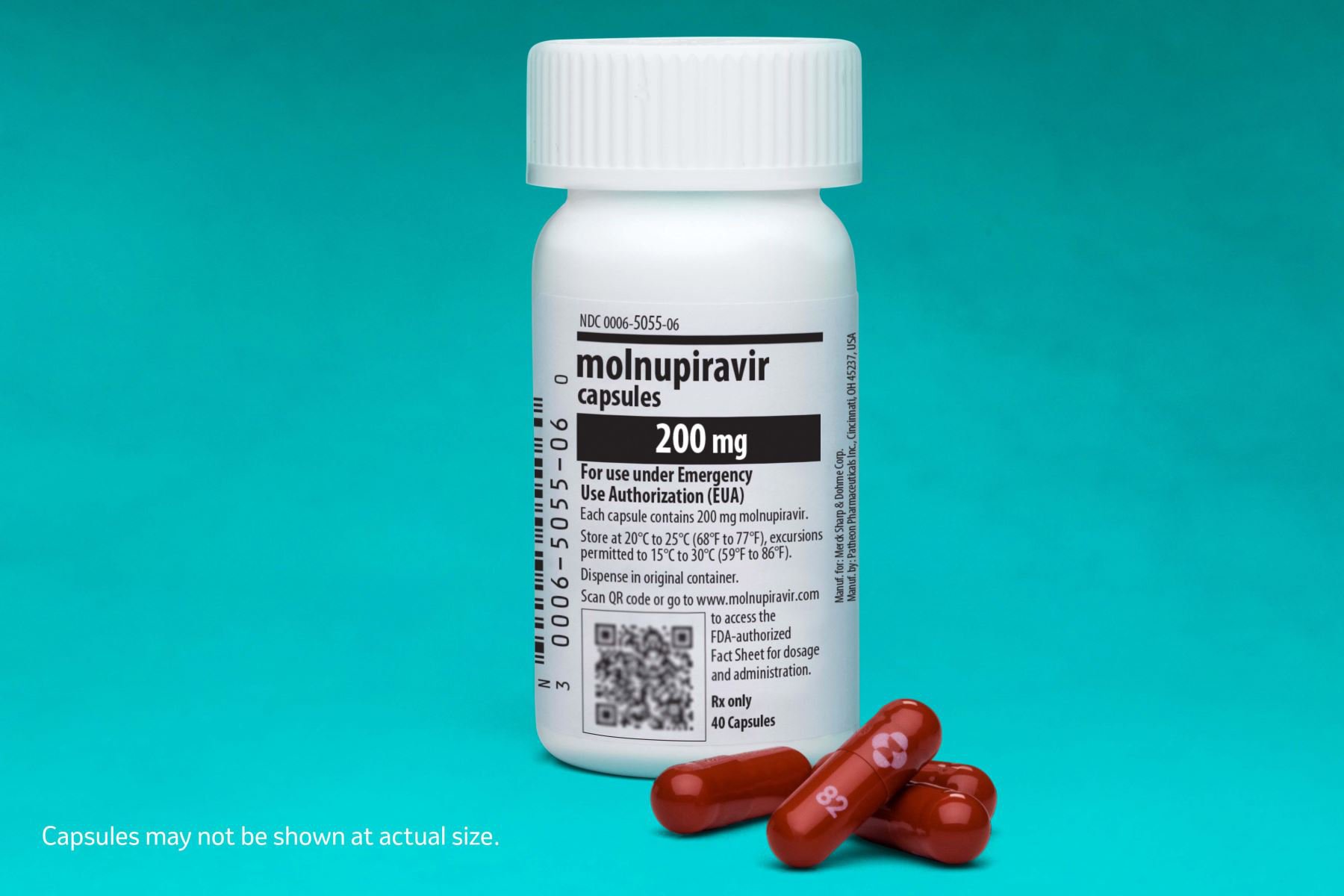
El molnupiravir, el primer medicamento oral creado para tratar la covid-19, ha sido autorizado en Perú por un año. El 15 de febrero, la Dirección General de Medicamentos, Insumos y Drogas (Digemid) le otorgó el registro sanitario condicional, lo que significa que podrá ser comercializado en cualquier establecimiento médico del país. En más de diez países esta medicina también ha recibido la aprobación para su uso; sin embargo, existen cuestionamientos respecto a su eficacia y seguridad que deberíamos tomar en cuenta antes de adquirirla.
Todo lo que se sabe hasta ahora sobre el molnupiravir se basa en un único estudio, realizado por la farmacéutica Merck Sharp & Dohme (MSD), precisamente la que ha desarrollado este medicamento. El molnupiravir ha sido presentado como un antiviral recomendado para casos leves a moderados de covid-19. Si se toma durante cinco días, desde el inicio del primer síntoma, evitará la replicación del virus, por tanto, mantendrá una baja carga viral en el paciente y reducirá la posibilidad de que enferme gravemente. También, se ha dicho que sería efectiva ante las nuevas variantes que puedan aparecer con el paso del tiempo. Dean Y. Li, presidente de los laboratorios de Investigación de MSD, dijo que la píldora tiene “una actividad antivírica consistente contra ómicron”.
Los cuestionamientos inician desde el reclutamiento de sus voluntarios: los más de 1400 pacientes de diversas partes del mundo que integraron este estudio no habían recibido ninguna vacuna contra la covid-19 cuando se inscribieron como participantes. Actualmente, en nuestro país, el 80% de la población está inmunizada con dos dosis; entonces, ¿la eficacia de esta medicina será la misma que en una población no vacunada? “Si habría algún beneficio, se daría en una cantidad mucho menor a la que se encontró en el ensayo”, dice el epidemiólogo Álvaro Taype-Rondán.
Para Leonardo Arregocés, director de Medicamentos del Ministerio de Salud de Colombia, país que también ha autorizado el uso de la píldora, se espera que en las siguientes semanas se tengan más datos claros sobre la eficacia del molnupiravir en vacunados, ya que en más de diez países se usa en estas poblaciones.
Un segundo problema es su eficacia. En octubre del 2021, a través de una nota de prensa, MSD dio a conocer los resultados preliminares de su estudio, en el que aseguró que fue suspendido antes de lo previsto debido a las cifras positivas obtenidas respecto a la eficacia del antiviral. En ese momento, se dijo que el molnupiravir demostró una eficacia del 50% frente a la reducción de hospitalización y muerte por coronavirus. Unos meses después, cuando el estudio fue publicado en la revista científica The New England Journal of Medicine, se comunicó que el porcentaje se redujo al 30%.
El epidemiólogo Álvaro Taype-Rondán explica que a veces los ensayos clínicos pueden suspenderse porque los investigadores van revisando los datos y en un punto parecen encontrar resultados importantes que consideran suficientes para el estudio. Pero esta suspensión temprana “usualmente se asocia a una sobrestimación de beneficios”.
De cualquiera forma, estas cifras son menores a las que demostró el laboratorio Pfizer sobre su píldora oral llamada Paxlovid, que también ha desarrollado para el tratamiento del coronavirus y ha sido aprobada en algunos países, aunque no en Perú. De acuerdo con sus comunicados de prensa, esta medicina logró una disminución de la muerte y hospitalización del 87% en comparación con los pacientes que recibieron placebo.
Las dudas sobre la seguridad de la medicina también han surgido luego de conocer que el molnupiravir no está recomendado durante el embarazo, ni para quienes están amamantando, porque se han reportado daños en los fetos de animales gestantes que recibieron esta medicina. Por eso, también se indica que las mujeres que decidan tomar la píldora, deberán realizarse una prueba de embarazo antes o usar métodos anticonceptivos constantes hasta cuatro días después de haber tomado la última dosis de molnupiravir. En el caso de hombres sexualmente activos, también se recomienda el uso de anticonceptivos hasta cuatro meses después de ingerir la última dosis.
“Al autorizarse el molnupiravir podría darse una libre compra para todos los usuarios. Entonces, no creo que alguien se haga una prueba de embarazo previa cada vez que desea tomar este medicamento para prevenir algún efecto secundario”, cuestiona el epidemiólogo Álvaro Taype.
Además de estos efectos, se han registrado algunos voluntarios que presentaron diarrea, náuseas y mareos luego de tomar el molnupiravir. En general, esta medicina indica que no está recomendada en menores de 18 años, personas hospitalizadas por coronavirus y tampoco puede ser usada como método de prevención de esta enfermedad.
Sin embargo, hay algunos resultados positivos. El ensayo reclutó a personas mayores de 18 años, con covid-19 sintomático (que previamente habían confirmado tener el virus con una prueba PCR) y con algún factor de riesgo para la progresión de la enfermedad, a quienes se les dio seguimiento durante 29 días. Es decir, la píldora sí está recomendada en pacientes con diabetes, obesidad, problemas cardíacos, enfermedad renal, cáncer o adultos mayores.
Si bien el estudio de Merck Sharp & Dohme ha sido el que ha servido para que diversos países, incluido el nuestro, lo apruebe para su comercialización y uso, de acuerdo a la plataforma Clinical Trials, hay al menos otras siete investigaciones en proceso. En cuatro de ellas aún se sigue reclutando a los voluntarios. Sin embargo, de las que ya han ofrecido resultados se supo que fueron realizadas con pocos participantes que tampoco habían recibido ninguna vacuna contra la covid-19. Desde MSD también han iniciado otro ensayo que estudia la eficacia y seguridad del medicamento en la prevención de la covid-19 dentro de los hogares. Los resultados aún no han sido publicados.
Hasta el momento, el ministro de Salud, Hernán Condori, ha negado que Perú vaya a incluir el molnupiravir dentro del protocolo actual de tratamiento contra la covid-19 por su “baja eficacia”.
Otros cuestionamientos
El mulnupiravir viene en una caja de 40 píldoras de 200 mg. cada una. La dosis recomendada para un adulto mayor de 18 años es de 800 mg cada 12 horas (ocho píldoras diarias) por cinco días a partir de la aparición del primer síntoma. Pero, ¿qué ocurre con las personas que, pese a tener síntomas, no acudieron a tomarse una prueba covid-19?
“Si bien hemos aumentado la capacidad de diagnóstico con pruebas PCR y los laboratorios pueden entregar resultados en 24 o 48 horas, ¿podremos disminuir esos tiempos para tener un diagnóstico más rápido?”, se pregunta Paola Páez, médica cirujana y especialista en Bioética en una entrevista al diario El Espectador de Colombia. Esta situación es muy similar a la que ocurre en nuestro país, donde aún hay demoras en la entrega de resultados de las pruebas de detección covid-19 ante la falta de personal y de laboratorios que las procesen.
Hay que tomar en cuenta además que la gran mayoría de personas solicita ayuda en un establecimiento de salud cuando la enfermedad empieza a agravarse, un momento en que el molnupiravir ya no sería eficaz.
“Nuestro presupuesto para la salud es limitado, pese a que se ha hecho un esfuerzo durante la emergencia por la pandemia. Estamos en este escenario donde hay presión por comprar fármacos nuevos y caros de manera masiva, pero esa decisión debe ser tomada con racionalidad. Para aprobar un fármaco, debemos primero verificar su eficacia y luego ver si esto no nos retirará presupuesto para otras medidas que sí han demostrado efectividad, como las campañas de vacunación o las mejoras el primer nivel de atención”, recomienda el epidemiólogo Taypre-Rondán, quien asegura que en Estados Unidos cada tratamiento completo del molnupiravir tiene un valor de 700 dólares.
De acuerdo al ministro de Salud, aún no se ha tenido una conversación con Merck Sharp & Dohme sobre el costo de la píldora.