La urgencia por encontrar una terapia eficaz para controlar y vencer la enfermedad respiratoria COVID-19 ha generado cientos de investigaciones y experimentos en el mundo. Pero hay uno que ha despertado altas expectativas por su tamaño: Solidarity, un ensayo clínico multicéntrico liderado por la Organización Mundial de la Salud (OMS) y al que se han sumado por lo menos 74 países para probar con pacientes hospitalizados cuatro terapias farmacológicas. Estas incluyen las medicinas remdesivir, cloroquina e hidroxicloroquina, ritonavir/lopinavir, ritonavir/lopinavir + Interferón-Beta.
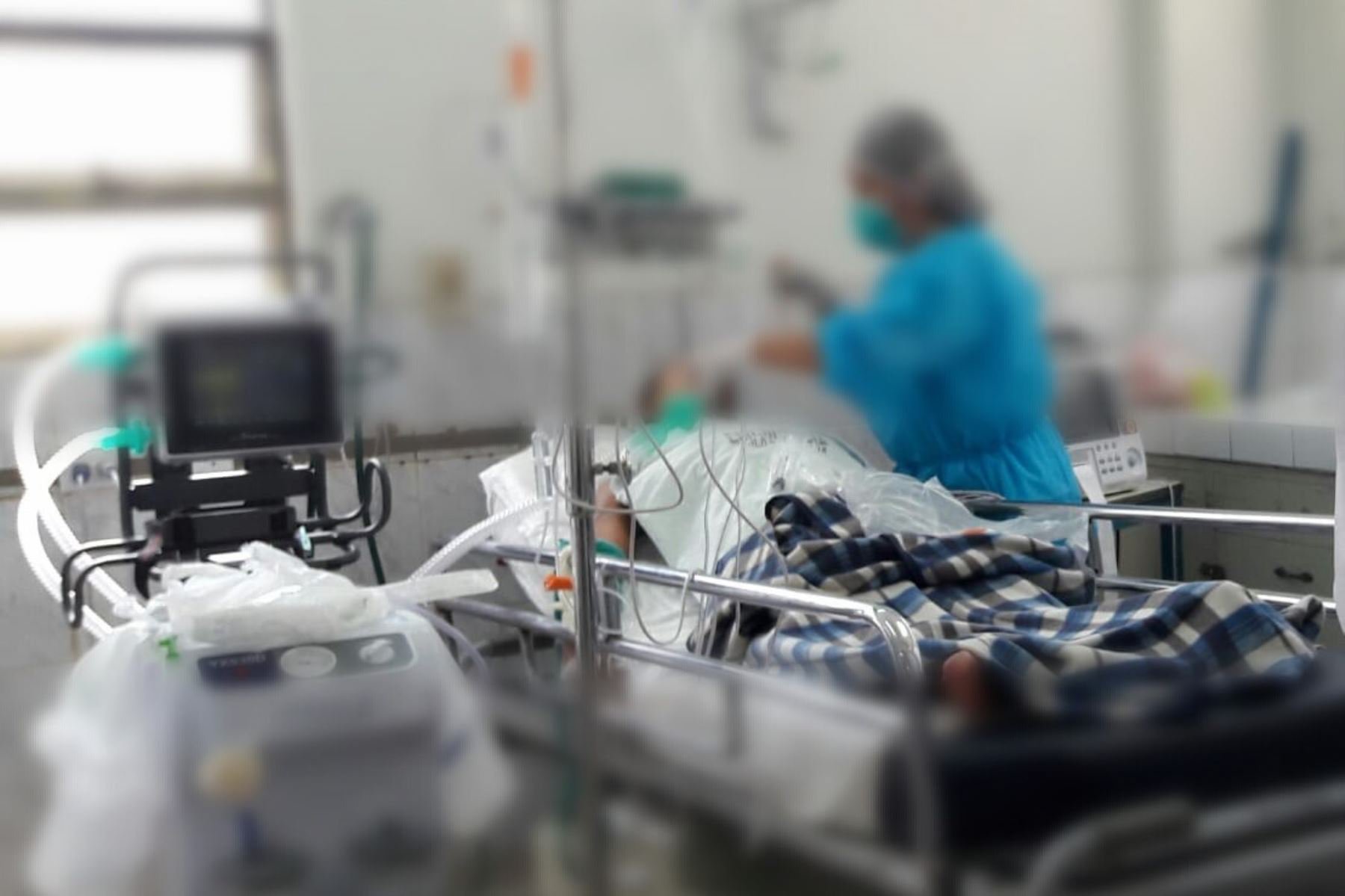
El pasado 28 de marzo, el Perú solicitó ser incluido en esta investigación a través de una carta enviada al director general de la OMS, Tedros Adhanom, en la que comunica que “se han tomado todas las acciones necesarias para facilitar los procesos del ensayo en el menor tiempo posible en hospitales y clínicas del país”. Salud con lupa conoció que pacientes atendidos en el hospital de Ate, habilitado para los enfermos de COVID-19 en Lima, así como en los hospitales Cayetano Heredia y Guillermo Almenara y las clínicas San Felipe, Anglo Americana y San Pablo, participarán en este ensayo clínico. El número de servicios de salud que serán centros de investigación irá creciendo, según fuentes del Instituto Nacional de Salud.
Aunque todavía no aparece en el registro oficial de ensayos clínicos del país, la investigación denominada “Ensayo Clínico Aleatorizado Internacional para Evaluar Tratamientos No Licenciados para COVID-19 en Adición a Cuidados Estándar en Pacientes Hospitalizados” estárá a cargo de la epidemióloga y exministra de Salud, Patricia García, y el infectólogo Eduardo Gotuzzo, investigador y experto en Salud Pública. Ambos supervisarán el enrolamiento de los pacientes y registrarán su evolución. Solo se probarán medicamentos con personas mayores de 18 de años con diagnósticos confirmados de COVID-19.
¿En qué consiste Solidarity?
Se trata de un ensayo clínico que nace en el Oslo University Hospital y está respaldado por la Organización Mundial de la Salud (OMS) por el tamaño de la muestra. Al principio, se estimaba la participación de 700 pacientes severos de COVID-19, pero con la adhesión voluntaria de decenas de países la población estudiada será mucho mayor. “Es posible que múltiples ensayos pequeños con diferentes metodologías no brinden la evidencia clara y sólida que necesitamos sobre qué tratamientos ayudan a salvar vidas, pero hay mayores posibilidades con un estudio grande”, dijo el director general de la OMS, Tedros Adhanom, cuando dio a conocer la investigación en una conferencia el 18 de marzo.
El diseño de Solidarity estuvo pensado para 10 países: España, Bahrein, Canadá, Francia, Irán, Noruega, Sudáfrica, Suiza, Tailandia y Argentina. Sin embargo, el 27 de marzo, la OMS anunció que otros 35 países se habían unido a la prueba o habían mostrado interés en hacerlo. “Cuantos más países se unan, más rápido tendremos resultados”, dijo Adhanom.

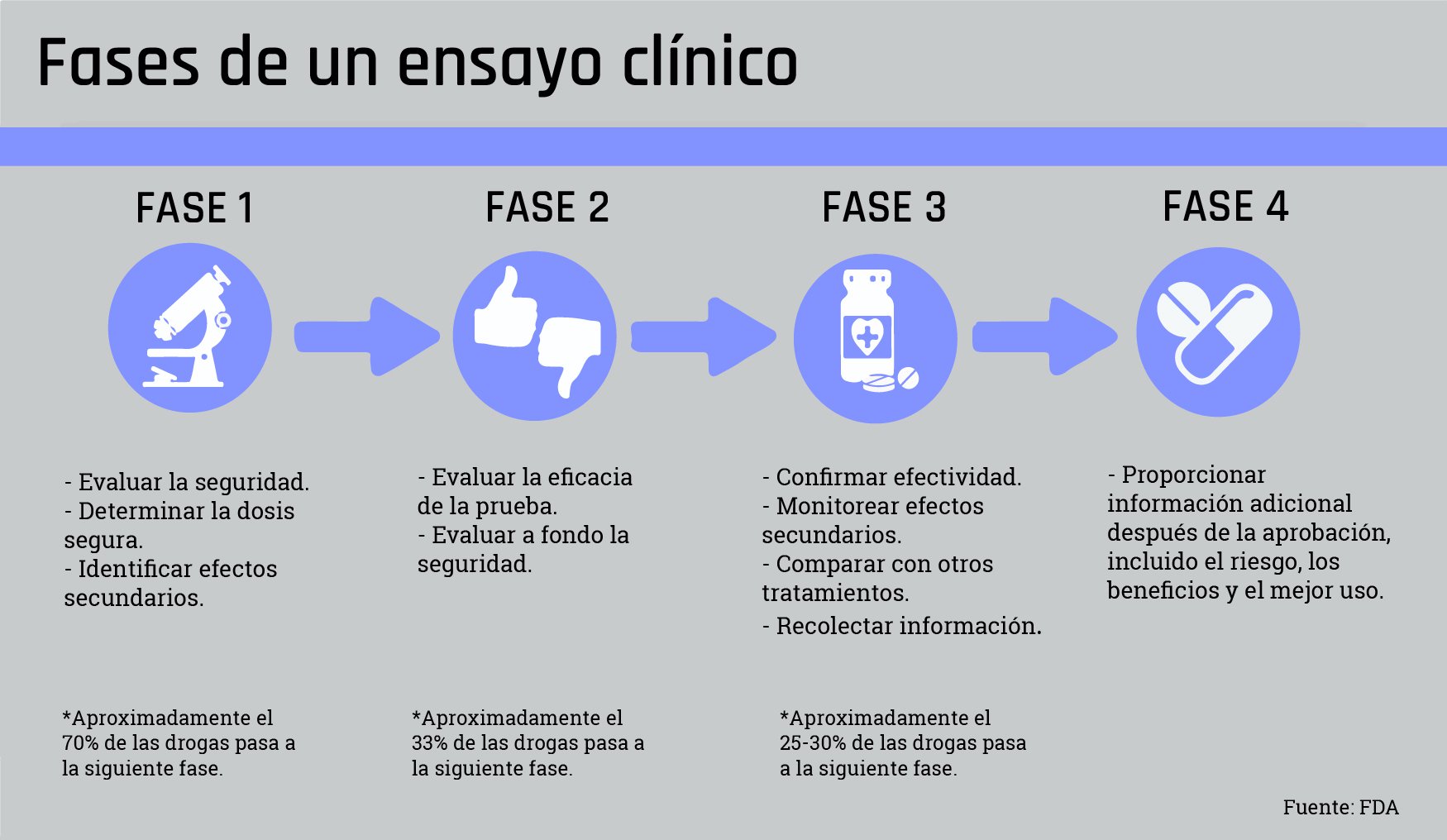
El ensayo clínico ha sido organizado en apenas semanas para enfrentar la situación de emergencia y finalizará en noviembre de 2020. Por eso, se han simplificado las fases convencionales de los estudios clínicos. Según la OMS, “ha sido necesario reducir cierto rigor científico en favor de la velocidad”.
Solidarity es un ensayo clínico aleatorizado (se seleccionará a los pacientes candidatos en forma aleatoria), de método abierto (investigadores y participantes enrolados conocen el tratamiento que se está administrando) y controlado (un grupo de pacientes recibirá los medicamentos en estudio y otro no).
Hasta la fecha, no se ha divulgado el número de pacientes enrolados en Solidarity, pero se conoce que su selección tampoco tendrá el proceso habitual. Ambos factores podrían dificultar la interpretación de la información, pero se confía en que un número muy elevado de personas que está probando las medicinas ayudará al análisis y corregirá posibles distorsiones.
¿Qué medicinas están en el ensayo?
Son fármacos en cuatro posibles tratamientos:
- Remdesivir
Es una terapia antiviral, desarrollada originalmente para el ébola por la farmacéutica estadounidense Gilead Sciences, que posee patentes sobre el fármaco en más de 70 países de todo el mundo. Este medicamento no dio buenos resultados para tratar la enfermedad para la que fue creada cuando se probó en la República Democrática del Congo durante 2018 y 2019. Sin embargo, sí ha mostrado su eficacia en el laboratorio contra el virus del SARS y el MERS, que también causa infecciones respiratorias.
Según una publicación de la revista New England Journal of Medicine (NEJM), remdesivir fue el tratamiento que se escogió para tratar al primer paciente diagnosticado de COVID-19 en los Estados Unidos y que empeoró sus síntomas. Un día después de haberle suministrado el tratamiento, su estado de salud mejoró. Lo mismo ocurrió con otros pacientes en los que se probó esta terapia. No obstante, estos casos solo se han considerado anecdóticos y se deben realizar ensayos clínicos que validen la eficacia del medicamento.
El investigador de la Universidad de Iowa Stanley Perlman explicó a Science que remdesivir parece seguro y que aunque aún no se sepa su precio es previsible que será caro. La farmacéutica Gilead Sciences logró la aprobación rápida del fármaco como medicamento huérfano, una designación especial de la FDA que le iba a permitir ventajas comerciales que podrían limitar su disponibilidad. Sin embargo, tras las críticas de la sociedad civil, Gilead renunció a su solicitud.
El último lunes 30 de marzo, 145 organizaciones de la sociedad civil enviaron una carta a Gilead para que se abstenga de reclamar las patentes que tiene en 70 países de su antiviral. Si no lo hace, podría generar un monopolio que pondría en riesgo la accesibilidad de remdesivir para millones de personas.
- Cloroquina e Hidroxicloroquina
La cloroquina es un medicamento utilizado para el tratamiento de la malaria. Se usa también para combatir la colitis amebiana, causada por el parásito Entamoeba histolytica. Se vende desde hace 70 años y está disponible en pastillas bajo la marca comercial de Aralen y también tiene una versión genérica.
Mientras que la hidroxicloroquina es un antimalárico que puede utilizarse para tratar la artritis reumatoide leve o en combinación con otras drogas para el tratamiento de enfermedades más graves. Además, se ha aplicado en pacientes con lupus que sufren complicaciones.
El uso de cloroquina e hidroxicloroquina para el tratamiento de COVID-19 ha sido recomendado por algunos profesionales de la salud basados en resultados de estudios in vitro (pruebas de laboratorios sin animales). Sin embargo, no se dispone de resultados de ensayos clínicos aleatorios (estudios con dos grupos grandes de personas: uno que recibe el tratamiento y otro que no lo hace) o estudios observacionales sobre su eficacia, efectividad y seguridad en pacientes con el nuevo coronavirus. Según la OMS, hay algunos indicios de que podría ser útil, pero no hay estudios claros y rigurosos que se hayan realizado para probar o refutar su efectividad.
Actualmente, no es muy difícil conseguir cloroquina. Después de que el presidente de Estados Unidos, Donald Trump, se refiriera a este fármaco como un medicamento revolucionario para luchar contra la pandemia, su país sufrió un desabastecimiento de esta droga, según alertó la Sociedad Estadounidense de Farmacéuticos Hospitalarios.
En el Perú, el nuevo protocolo de prevención y atención a personas afectadas por COVID-19 señala que se acogerá la propuesta de poner a consideración de los médicos especialistas y bajo su responsabilidad, los esquemas de tratamiento que las sociedades científicas nacionales han sugerido. Estas incluyen cloroquina, hidroxicloroquina y la combinación de hidroxicloroquina y azitromicina.
Estas opciones de tratamiento deben ser explicadas al paciente para que brinde su consentimiento informado de que se somete a un tratamiento en ensayo clínico y solo se considerarán casos moderados o severos; es decir, solo para pacientes hospitalizados.
- Ritonavir/Lopinavir o Kaletra
Los antirretrovirales combinados ritonavir/lopinavir, cuyo nombre comercial es Kaletra, previenen que el VIH se multiplique en el cuerpo de un infectado.
Algunos especialistas han empezado a recomendar el uso de tratamiento de estos antivirales para combatir la enfermedad de COVID-19 basados en la experiencia ganada durante la epidemia de SARS del 2002. Las guías prácticas clínicas internacionales aún no brindan recomendaciones homogéneas respecto al uso de kaletra en los pacientes con el nuevo coronavirus. Las guías de los Centros para el Control y Prevención de Enfermedades (CDC) y de la Organización Mundial de la Salud (OMS) no han realizado alguna recomendación respecto a su uso como tratamiento. Sin embargo, Kaletra es una de las cuatro medicinas que entrarán al estudio clínico Solidarity.
- Ritonavir/Lopinavir más Interferón-Beta
Otro de los grupos de tratamiento del ensayo clínico incluye interferón-beta y ritonavir/lopinavir.
El interferón alfa 2b es una sustancia que se elabora normalmente de las células del sistema inmunitario y se produce en un laboratorio. Este fármaco de tecnología cubana se usa para el tratamiento de un tipo de leucemia. El medicamento ha sido usado en China para tratar a algunas personas con COVID-19.