Al empezar la pandemia, arrancó también una carrera frenética de los laboratorios por encontrar un tratamiento y una vacuna efectiva contra el COVID-19. Sin embargo, por enfocarnos en la cura, prestamos menos atención a algo tanto o más urgente: las herramientas de diagnóstico y prevención. A seis meses de emergencia sanitaria en nuestro país, los casos de infecciones siguen en aumento por lo que es necesario evaluar la calidad de pruebas de diagnóstico en las que estamos confiando.
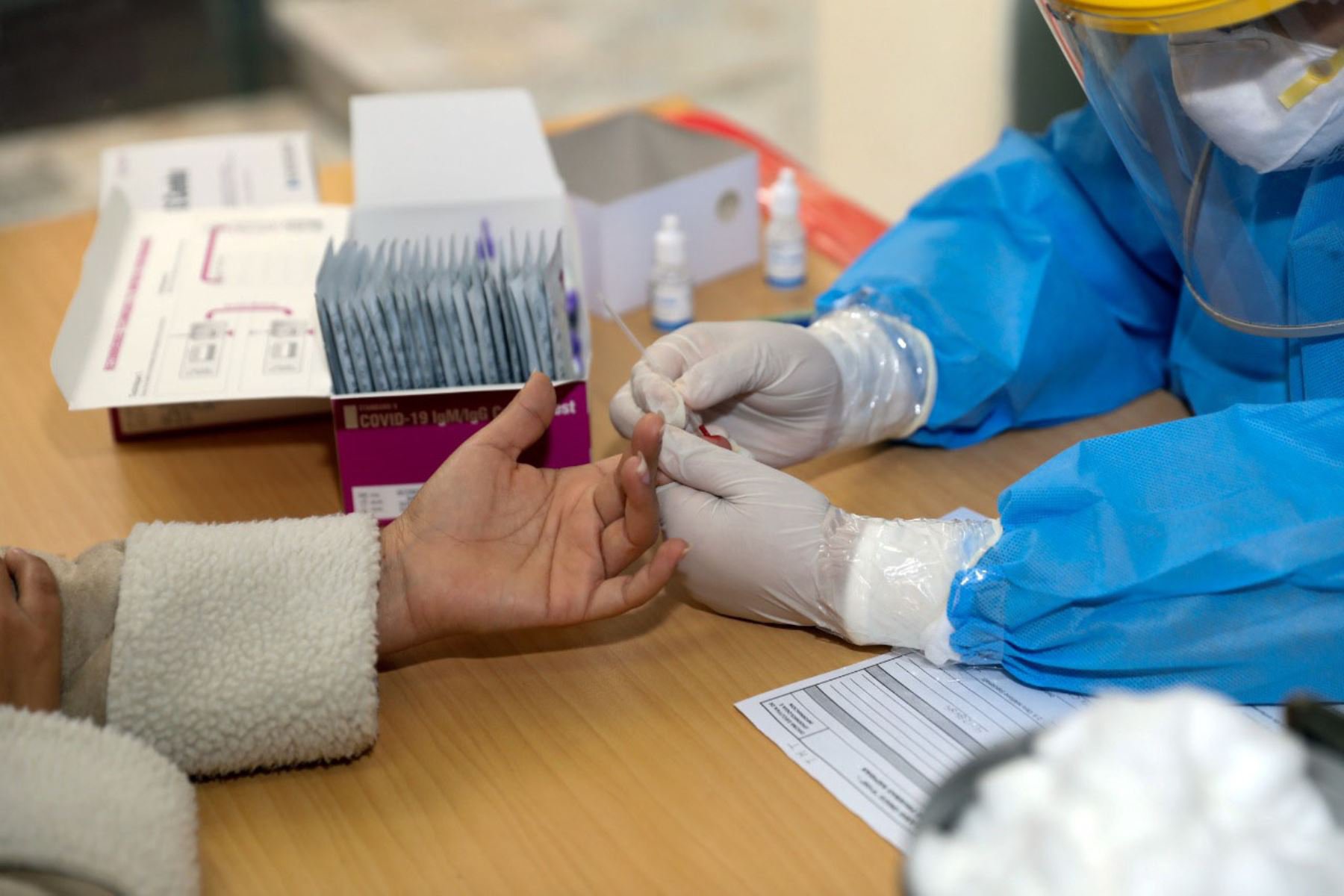
La prueba más eficaz para saber si uno tiene COVID-19 es la molecular o PCR, que detecta partículas del ARN del coronavirus en nuestro organismo. En el Perú estas son escazas porque necesitan de insumos y reactivos que debemos importar de otros países. Además exigen ciertas condiciones en los laboratorios y personal capacitado para procesarlas. Por eso, desde un inicio se optó por utilizar las pruebas serológicas, también conocidas como pruebas rápidas. Estos análisis, mediante una muestra de sangre, detectan la presencia de anticuerpos al coronavirus. Son más económicos y veloces que las moleculares, pero su margen de error es más amplio.

“Con datos errados, las personas tienen una falsa sensación de seguridad y exponen a otros a la transmisión del virus”, comenta el doctor César Ugarte-Gil, docente de la Universidad Peruana Cayetano Heredia e investigador del Instituto de Medicina Tropical Alexander von Humboldt. Por eso, actualmente Ugarte-Gil lidera uno de los primeros estudios de validación de pruebas de diagnóstico de COVID-19 en el país que busca definir cuáles son las que puedan otorgar resultados con mayor seguridad y según qué circunstancias.
Tenemos más de 560 mil casos positivos de COVID-19 ¿se justifica todavía el uso de pruebas rápidas?
No, porque lo que necesitamos es encontrar a pacientes con enfermedad activa y que no sigan transmitiendo. Para eso se requiere pruebas moleculares.
Si urge detectar casos, buscar y hacer seguimiento a sus contactos ¿Cuál es la estrategia por seguir?
Aumentar nuestra capacidad de pruebas moleculares, lo que implica ver dónde están las barreras para llegar a más personas sospechosas de tener la infección. Solo el hecho de entregar el resultado en 24 horas de una prueba molecular y aislar a la persona positiva, disminuye en un porcentaje considerable la transmisión en la comunidad.
¿Por qué optamos al inicio de la pandemia por las pruebas rápidas?
Había que usar lo que estaba a la mano mientras se desarrollaba capacidad para hacer pruebas moleculares. Como van los casos, no podemos dejar de pensar en estrategias diagnósticas por pensar solo en vacunas y tratamiento. Necesitamos hacer pruebas de diagnóstico, seguimiento y rastreo de contactos y, para lograrlo, tenemos que ser más activos de lo que hemos podido ser, por ejemplo, con la búsqueda de contactos de personas con tuberculosis, algo que se hace desde mucho tiempo atrás.
Es un gran esfuerzo logístico.
Lo es. Implica tomar pruebas diagnósticas a gran escala ¿Qué opciones tenemos? La historia natural de la enfermedad demuestra que las pruebas PCR, las moleculares, sirven solo en la primera semana de síntomas. Recién a partir de entonces, las pruebas serológicas van a salir positivas. El uso de pruebas diagnósticas debe ser racional. No se trata de testear por hacerlo. Cada prueba tiene sus debilidades y fortalezas. La única manera de controlar la pandemia es realizar pruebas moleculares.
La ministra de Salud, Pilar Mazzetti, anunció la semana pasada que dejarán de usar, poco a poco, las pruebas rápidas.
Tiene que ser poco a poco porque para una prueba molecular se necesitan insumos, reactivos, un determinado tipo de hisopo. Y están escasos a raíz de la pandemia. Hay que validar, incluso, los hisopos. De no hacerlo, la muestra no servirá y el resultado puede salir negativo.
¿Cuáles son los reactivos que faltan y cómo esto afecta el control de la pandemia y la investigación?
Faltan varios reactivos: kit de extracción de ARN, medios de transporte viral, hisopos, etc. Además, el Perú no suele ser un país que compre muchos de estos materiales, así que todo debe ser importado y no hay un stock. Una de las enseñanzas de esta pandemia es que, como parte de la seguridad nacional, se debe mantener una reserva de ese material o producir localmente. A veces, olvidamos que el Perú es un mercado pequeño. Cuando compites con compañías y países grandes, no eres económicamente atractivo para comprar, a pesar de que el país ha pedido adquirir cantidades industriales de pruebas de detección para COVID-19.
Las pruebas rápidas son las más utilizadas por los empleadores para reabrir sus negocios.
Personalmente no le encuentro sentido a sacar pruebas rápidas a la gente que trabaja porque varios van a salir negativos, a pesar de ser positivos.Tenemos que preguntarnos qué pruebas estamos usando. Lamentablemente, hay un mercado invadido por pruebas serológicas de muy buena y de muy mala calidad. Asumo, por lo general, que quien sale positivo una vez, es porque ha tenido la infección. Sin embargo, podría haber reacciones cruzadas.
Los estudios de seroprevalencia realizados en Loreto, Lima, Cusco han utilizado pruebas rápidas.
La función de las pruebas serológicas no es hacer tamizaje sino estudios de seroprevalencia. Pero al no haber pruebas rápidas bien validadas, es recomendable recurrir también a la prueba de ELISA para determinar la prevalencia real. Para realizarla se requiere de un laboratorio de inmunología y un tubo de muestra sanguínea. Con este tipo de muestra de sangre también aumenta la sensibilidad de las pruebas rápidas. Pero en la calle o en un paradero de buses no te puedes dar ese lujo. Por eso, es importante tener pruebas serológicas que funcionen.
Usted lidera un estudio de validación de pruebas de diagnóstico de COVID-19 ¿En qué se diferencia del trabajo del Instituto Nacional de Salud?
El mercado se ha llenado de pruebas rápidas y necesitamos saber cuáles realmente son las mejores. Sé que el Instituto Nacional de Salud realiza validaciones internas. Es un control de calidad en el laboratorio de un lote determinado de pruebas. El estudio que vamos a iniciar en el Instituto de Medicina Tropical Alexander von Humboldt de la Universidad Peruana Cayetano Heredia verificará la sensibilidad y especificidad de estos instrumentos fuera del laboratorio, en pacientes reales. Buscamos evidencia que permita hacer un uso racional de las pruebas de diagnóstico. Sobre todo, ahora, que disponemos de más datos sobre la variedad clínica de la enfermedad.
¿Qué características van a evaluar?
Queremos evaluar las pruebas en diferentes tipos de pacientes (severos y no severos, ambulatorios y hospitalizados) porque eso permite validar sus diferentes respuestas inmunológicas. Queremos tener pruebas que funcionan en la vida real y en la diversidad de condiciones de los establecimientos de salud donde se aplican, como humedad, electricidad inestable, calor, polvo. La prueba molecular, por ejemplo, es muy sensible a humedad y temperatura. Hay que tener mucho cuidado con la técnica al tomar la muestra del hisopado. Además, en los estudios clínicos de la vacuna contra el COVID-19 se requerirá de pruebas de diagnóstico validadas clínicamente.
¿En qué consiste el estudio clínico?
Hemos pedido permiso para enrolar a unas 500 personas para tener la capacidad de escoger una variedad amplia de diferentes presentaciones clínicas y, en función de eso, analizar la precisión diagnóstica de cinco pruebas serológicas. Examinaremos, asimismo, cinco pruebas de antígenos. Todo esto con apoyo de la organización FIND. En otro estudio con 500 a 600 voluntarios, evaluaremos la prueba XpertXpress Sars-Cov2. Para esta última línea de investigación tenemos el apoyo de Canadian Institutions of Health Research, en colaboración con la Universidad McGuil de Canadá.
¿Los voluntarios serán pacientes del hospital Cayetano Heredia?
Tenemos todos los permisos para llevar a cabo esta investigación. Enrolaremos a pacientes que acudan al hospital Cayetano Heredia con síntomas de COVID-19. La tercera parte de ellos serán pacientes hospitalizados, y las dos terceras partes, pacientes ambulatorios con síntomas moderados de la infección. Se les tomará una muestra de sangre y un hisopado nasofaríngeo.
¿Cuántas pruebas serán validadas?
Empezaremos por definir la precisión diagnóstica de cinco pruebas serológicas (incluye las que utilizan gota de sangre), aunque la meta es probar veinte tipos de pruebas. El estudio es financiado por FIND, una organización que coordina entre los grupos de investigación y los fabricantes de pruebas diagnósticas interesados en realizar investigaciones de validación. Con esta organización, que también coopera con la OMS por la pandemia, hemos trabajado en los últimos 14 años en la validación de pruebas diagnósticas para tuberculosis y malaria.
Tengo entendido que el grupo de pacientes con pruebas serológicas se les hará seguimiento durante dos meses.
Las pruebas serológicas están diseñadas para detectar anticuerpos. Estos aparecen en los primeros días de la infección, pero decaen aparentemente en número con el paso de los días. Los kits se desarrollan pensando en una cantidad límite de anticuerpos. Por eso, el estudio contempla que a un grupo de pacientes se aplique la prueba serológica en diversos momentos, durante dos meses. Necesitamos saber hasta qué fecha funcionan los kits por validar.
¿Cuál será el patrón de referencia o de comparación de resultados?
La prueba molecular PCR será el Gold-standard. Para realizarla, tomaremos a los pacientes un hisopado nasofaríngeo. La muestra respiratoria servirá también para evaluar de cuatro a cinco pruebas de antígenos (detectan proteínas glucanos, como la proteína espiga presente en la superficie del nuevo coronavirus) porque queremos comparar su rendimiento diagnóstico con el de la prueba estándar (prueba molecular). Esa información permitiría escoger la mejor prueba de antígenos para usar.
También estudiarán la viabilidad de una pruebade diagnóstico que funcione para COVID-19 y tuberculosis.
Es otra línea de investigación. Consiste en evaluar el sistema Xpert Xpress Sars-Cov2. Esta es una prueba diagnóstica molecular in vitro que permite la detección y diagnóstico del ARN del virus del COVID-19 con PCR en tiempo real. Para ese fin, se usan muestras de hisopos nasofaríngeos, hisopos nasales o aspirado. Además de confirmar su precisión de diagnóstico, evaluaremos la viabilidad de usar una sola muestra de esputo para detectar COVID-19 y tuberculosis. La meta es lograr un diagnóstico referencial para ambas afecciones. Nuestra responsabilidad es conseguir la mejor evidencia y tomar decisiones bien pensadas. Tenemos que hacerlo de manera estructurada, racional, consistente y sistemática, de lo contrario, no vamos a salir de la actual situación.