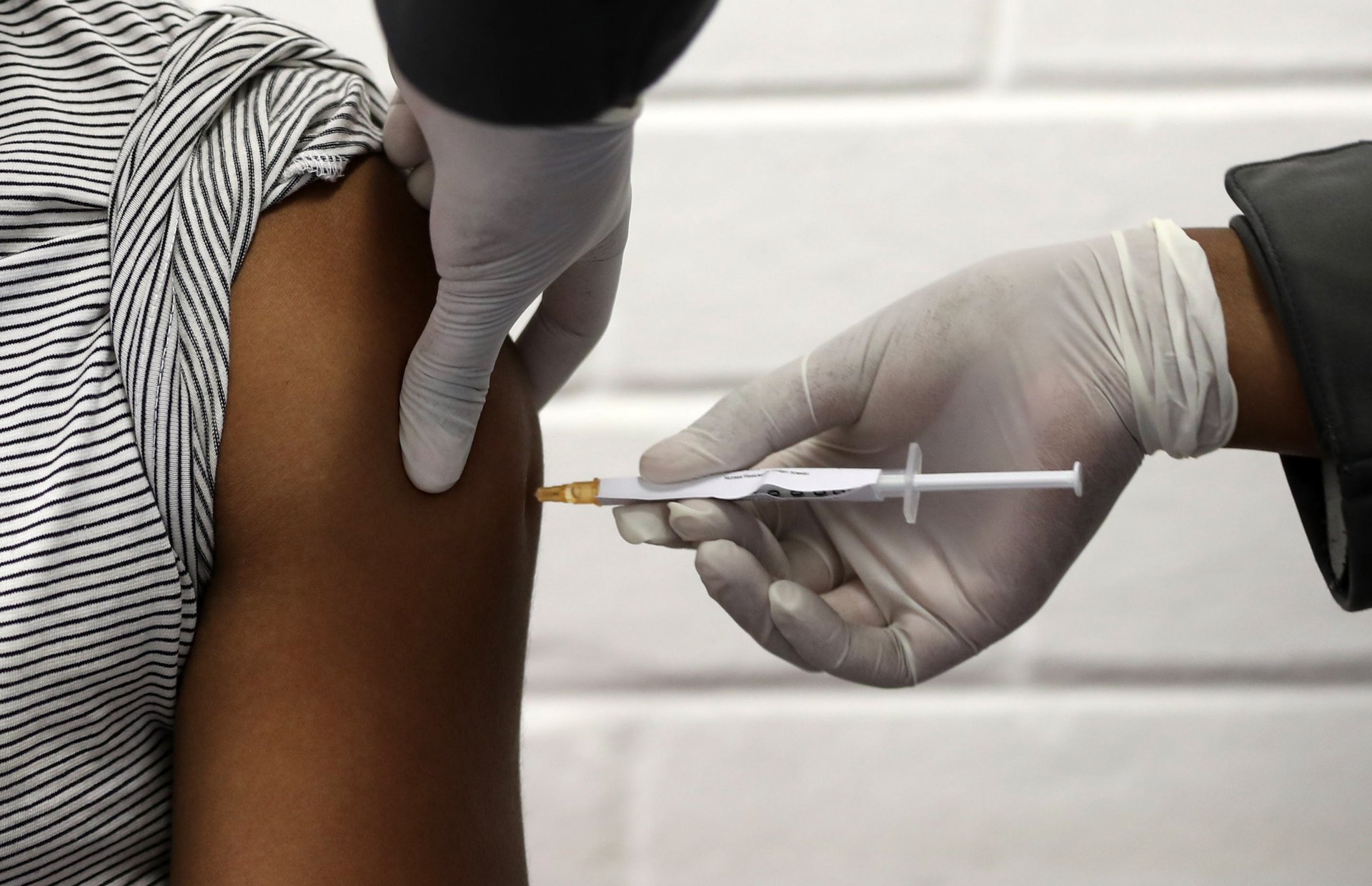
La Organización Mundial de la Salud (OMS) considera que una vacuna contra la COVID-19 debe aprobarse en función de los resultados obtenidos en la fase III de ensayos clínicos en la que participan miles de personas sanas para evitar abusar de los atajos que podrían afectar los datos sobre su verdadera eficacia y seguridad.
"Los científicos alrededor del mundo están pidiendo a las agencias reguladoras y a las compañías que la aprobación de una vacuna se haga en función de datos obtenidos en la fase 3", dijo la científica en jefe de la OMS, Soumya Swaminathan, en una rueda de prensa.
Sin embargo, Rusia ha anunciado que ya tiene lista una vacuna y que se prepara para vacunar a su población, a pesar de que acaba de entrar en la fase III de los ensayos. Mientras que China tiene avanzadas las investigaciones de dos vacunas que no han terminado la fase III, pero ha empezado a vacunar a sus trabajadores esenciales.
“La aprobación prematura de una vacuna implicaría riesgos”, dijo la pediatra y científica india Swaminathan. Uno muy concreto es que la vacuna aprobada con apuro tenga una eficacia muy baja, con lo cual "no haría su trabajo de poner fin a esta pandemia".
Entre los criterios acordados entre la OMS y las agencias reguladoras de algunos países donde se investigan vacunas experimentales está el nivel de eficacia que debería tener. La organización considera que debe ser de, al menos, un 50 % "y preferiblemente más alta".
A pesar de estos acuerdos, las autoridades sanitarias de Brasil han informado que trabajan para reducir los plazos de registro de la vacuna contra el nuevo coronavirus. El gerente de Medicamentos y Productos Biológicos de la Agencia Nacional de Vigilancia Sanitaria (Anvisa), Gustavo Mendes, dijo que se están preparando para aprobar una eventual vacuna en hasta 60 días, una vez que reciban toda la documentación necesaria.
El directivo de Anvisa, órgano vinculado al Ministerio de Salud brasileño, informó que un "comité de especialistas" ya discute los datos de las potenciales vacunas a medida que son generados, lo que facilitará el dictamen final de la entidad. "Normalmente recibimos un dossier completo con todos los datos para hacer el análisis, pero en una situación de pandemia los recibimos a medida que van siendo generados y así adelantamos nuestros análisis", explicó.
La OMS defiende que, a pesar de la urgencia que hay por encontrar una vacuna contra el COVID-19, se debe poner freno a cualquier vacuna experimental "con un perfil de seguridad que no sea aceptable".
"Lo más importante es que las decisiones se tomen en función de lo que dice la ciencia y contar con un grupo de científicos que no sea influenciado por ningún interés, que analice los datos y recomiende si una vacuna debe ser aprobada", sostuvo Swaminathan.
"El desafío al que nos enfrentamos ahora es que pasamos de vacunar cientos de personas (fase II de ensayos clínicos) a cientos de miles de personas (fase III). Necesitamos los resultados de eficacia y seguridad de estos estudios porque si empezamos a vacunar a millones de personas muy rápido podemos pasar por alto algunos efectos adversos", explicó el director de Emergencias de la OMS, Mike Ryan.
Con información de la Agencia EFE