Este reportaje forma parte de The Cancer Calculus, una serie liderada por el Consorcio Internacional de Periodistas de Investigación en la que participa Salud con lupa.
Mientras el presupuesto para terapias esenciales contra el cáncer se ha reducido en los últimos años, el Ministerio de Salud ha concentrado cientos de millones de soles en pocos medicamentos de alto costo.
Entre 2023 y 2025, cinco fármacos absorbieron el 81% del gasto nacional en medicamentos oncológicos. Uno de los principales fue el pembrolizumab, comercializado como Keytruda por Merck Sharp & Dohme (MSD), un tratamiento utilizado en varios tipos de cáncer que ayuda al sistema de defensa del cuerpo a reconocer y atacar las células cancerosas.
Solo este fármaco implicó un gasto de 172 millones de soles en ese periodo. Es uno de los más caros: cada paciente necesita alrededor de 34 viales, lo que eleva el costo a unos 250 mil soles por terapia. A ese precio, el Estado apenas cubrió a unos 990 pacientes, incluidos los previstos para este año.
El alcance es limitado. Y ha puesto en tensión la capacidad del sistema de salud para cubrir tratamientos oncológicos.
¿Quién es responsable por estas decisiones?
Esa responsabilidad recae en el Instituto Nacional de Enfermedades Neoplásicas (INEN), que en los últimos años ha asumido un rol central en estas decisiones. No solo es el principal centro público donde se atiende a miles de pacientes, sino que también define qué medicamentos se aprueban y cómo se usa el presupuesto público destinado al cáncer.

Ese poder se consolidó con el reglamento de la Ley Nacional del Cáncer en 2022.
Al revisar cómo se tomaron esas decisiones sobre el pembrolizumab en el INEN, aparece un patrón que evidencia conflictos de interés.
Diez oncólogos de la institución —algunos con cargos directivos— participaron en la elaboración y aprobación de los documentos técnicos que permitieron su uso en distintos tipos de cáncer en el sistema público. Todos eran investigadores en ensayos clínicos de ese mismo medicamento financiados por Merck Sharp & Dohme.
Esto significa que quienes evaluaron el pembrolizumab también trabajaban para la empresa que lo produce y participaron en decisiones técnicas que facilitaron su compra con recursos públicos.
Ninguno declaró ese vínculo en los documentos formalizados en cuatro resoluciones jefaturales del INEN, que han sustentado adquisiciones de pembrolizumab en volúmenes cada vez mayores a través de la central de compras del Ministerio de Salud.
Médicos con doble rol
El pembrolizumab salió al mercado en 2014 y se ha convertido en una de las principales fuentes de ingresos de Merck Sharp & Dohme. Sus ventas acumuladas superan los 162.800 millones de dólares, consolidando a la farmacéutica entre las más grandes del mundo.
Su alto precio —en algunos países mayor al valor de una onza de oro por dosis— ha limitado el acceso a quienes pueden pagarlo y ha obligado a los sistemas públicos de salud a decidir en qué pacientes usarlo y si su beneficio justifica su costo frente a otras alternativas.
No es un tratamiento para todos los pacientes. Su indicación depende del estadio de la enfermedad y de ciertas características del tumor, como la presencia de proteínas que permiten predecir la respuesta a esta terapia.
Cuando se cumplen estas condiciones, puede mejorar la supervivencia frente a tratamientos convencionales. Sin embargo, su beneficio varía según el tipo de cáncer y no es igual en todas las personas.
Por ello, su incorporación en el sistema público exige decisiones técnicas basadas en evidencia y libres de conflictos de interés. Más aún cuando se han documentado estrategias de Merck Sharp & Dohme para sostener el posicionamiento de este fármaco en distintos países, incluyendo la expansión de sus indicaciones incluso en escenarios de beneficio limitado y una fuerte inversión en vínculos con médicos y grupos de pacientes para influir en su uso, según las revelaciones de The Cancer Calculus, investigación liderada por el Consorcio Internacional de Periodistas de Investigación y en la que participa Salud con lupa.

En el Perú, el Instituto Nacional de Enfermedades Neoplásicas incorporó el pembrolizumab en el tratamiento de distintos tipos de cáncer, como pulmón, melanoma, cáncer de mama triple negativo y cuello uterino. El problema no radica en el fármaco, sino en el proceso: su inclusión se dio sin pasar por evaluaciones completas de costo y beneficio realizadas por instancias técnicas independientes.
Los diez médicos que elaboraron y validaron los documentos técnicos que sustentan su incorporación mantenían una relación sostenida con la farmacéutica que lo produce.
Al cruzar las cuatro resoluciones jefaturales del INEN que firmaron entre 2019 y 2024 con el Registro Peruano de Ensayos Clínicos, todos sus autores figuran como investigadores de Merck Sharp & Dohme en al menos 28 ensayos clínicos de pembrolizumab en el Perú.
Este doble rol se evidencia con claridad en varios casos, como muestra la gráfica que publicamos.
El INEN aprobó el pembrolizumab con médicos que trabajaban para Merck Sharp & Dohme
Los diez autores de los documentos técnicos que sustentaron compras millonarias eran investigadores de Merck Sharp & Dohme y participaron en al menos 28 ensayos clínicos de pembrolizumab en el Perú.
Uno de ellos es Luis Mas López, actual jefe del Departamento de Oncología Médica del INEN, quien presentó el pembrolizumab en Perú en una conferencia de prensa de Merck Sharp & Dohme en abril de 2016.
Fue investigador principal del estudio clave de la empresa para cáncer de pulmón en primera línea. Luego integró el equipo que elaboró el documento técnico que sustentó su uso en hospitales del Estado para esa misma indicación.
Más adelante, como director general de Servicios de Apoyo del INEN, participó en la resolución que amplió su uso al cáncer de mama triple negativo. En total, figura como investigador en seis ensayos clínicos de este fármaco en el Perú patrocinados por la misma compañía.
Luis Mas tampoco declaró su relación con Merck Sharp & Dohme cuando se presentó ante la comisión especial de vigilancia de la atención del cáncer en el Congreso, en marzo de 2025. En esa sesión, defendió que el INEN debía encargarse de aprobar las terapias de alto costo.

También cuestionó las decisiones de la Red de Evaluación de Tecnologías Sanitarias (RENETSA) del Ministerio de Salud, la instancia encargada de evaluar el costo y beneficio de los tratamientos antes de recomendar su incorporación y financiamiento en el sistema público. Tras cambios legales recientes, ese rol ha pasado a ser asumido por el INEN, sin el mismo nivel de evaluación independiente.
"¿Qué esperamos de las evaluaciones de tecnología sanitaria? Que faciliten el acceso a estos medicamentos, porque la salud del paciente mejora y nosotros nos hemos visto afectados por la toma de decisión, que no necesariamente está basada en médicos que entienden la complejidad de la salud del cáncer”, señaló. En su intervención, incluso destacó las bondades del pembrolizumab.
En el grupo también aparece Mivael Olivera Hurtado de Mendoza, médica del INEN e investigadora del ensayo clínico más importante de pembrolizumab para cáncer de cuello uterino de Merck Sharp & Dohme. Formó parte del equipo que redactó el documento técnico de la resolución jefatural para su inclusión en el sistema público.
Además, participaba en otros dos ensayos clínicos activos de la farmacéutica sobre pembrolizumab para la misma enfermedad mientras elaboraba ese informe. Olivera ha sido investigadora contratada por Merck Sharp & Dohme en siete ensayos de pembrolizumab realizados en el Perú.
Otro oncólogo involucrado es Víctor Castro Oliden, director general de Medicina del INEN desde 2024, quien firmó la resolución que aprobó el uso de pembrolizumab para cáncer de cuello uterino. En paralelo, figuraba como investigador principal de un ensayo clínico de ese mismo fármaco para esa indicación en un centro privado. En total, aparece en nueve ensayos financiados por Merck Sharp & Dohme, ocho de ellos como investigador principal.
Le siguen los médicos Marco Gálvez Niño y Natalia Valdiviezo Lama, quienes integraron los equipos que elaboraron los documentos técnicos para autorizar el pembrolizumab en cáncer de pulmón y de cuello uterino.
Gálvez Niño figura como investigador en siete ensayos clínicos de este medicamento patrocinados por Merck Sharp & Dohme, en los mismos tipos de cáncer que evaluó en los informes que ayudó a aprobar.
Valdiviezo Lama aparece en cuatro ensayos de la misma compañía, también en las indicaciones que contribuyó a autorizar. Uno de ellos seguía activo para cáncer de cuello uterino mientras se elaboraba la última resolución en la que participó.
La doctora Valdiviezo también se presentó ante la comisión especial del Congreso para defender que los oncólogos aprueben las terapias de alto costo. En esa instancia se presentó únicamente como presidenta de la Sociedad Peruana de Mastología y no mencionó su vínculo con Merck Sharp & Dohme.
“Muchas de estas drogas han sido evaluadas con resultados negativos; sin embargo, cuando nosotros comparamos esto con el escenario mundial, estas mismas drogas han sido evaluadas y aprobadas en muchas oportunidades por sociedades o normativas con mayor experiencia, que les han dado la validez adecuada”, declaró en marzo de 2025 al cuestionar las evaluaciones de RENETSA.

Otro caso es el del oncólogo Hugo Fuentes Rivera, quien entre 2018 y 2023 fue director ejecutivo del Departamento de Investigación del INEN. En ese mismo período, integró el grupo que elaboró el documento técnico que sustentó la resolución para autorizar el pembrolizumab en cáncer de mama triple negativo, la misma indicación que investigaba en un centro privado para Merck Sharp & Dohme.
También está Henry Gómez Moreno, exdirector ejecutivo del Departamento de Oncología Médica del INEN entre 2019 y 2021. Firmó las tres primeras resoluciones que autorizaron el uso del pembrolizumab para cáncer de pulmón, melanoma y mama triple negativo en el sistema público. En ese mismo período participó en dos ensayos clínicos financiados por Merck Sharp & Dohme. Mientras firmaba la aprobación para cáncer de mama, era además investigador principal de un ensayo con pembrolizumab sobre esa misma enfermedad en una clínica privada.
Las cuatro resoluciones jefaturales del INEN permitieron que, entre 2023 y 2025, su Comité Farmacoterapéutico —presidido por Karina Aliaga— aprobara el uso del fármaco para al menos ocho indicaciones tumorales. Con esas actas e informes, la Dirección de Farmacia y la Gerencia del INEN sustentaron ante la central de compras del Ministerio de Salud la adquisición de volúmenes cada vez mayores de pembrolizumab.
Este proceso deja expuesto un problema de fondo. Aunque la normativa no exige declarar conflictos de interés en documentos técnicos, en la práctica el INEN los ha usado como guías clínicas para definir adquisiciones de alto costo. En las guías clínicas, esa declaración sí es obligatoria, lo que evidencia un vacío en reglas clave para decisiones que involucran millones de soles.
Los médicos fueron contactados por Salud con lupa para conocer sus descargos. También se solicitaron entrevistas a la dirección general del INEN y se envió un cuestionario por correo. Sin embargo, hasta el cierre de esta investigación, no hubo respuesta.
Frente a estos hallazgos, Merck Sharp & Dohme envió un pronunciamiento por escrito en el que evitó responder preguntas clave. Negó cualquier irregularidad y aseguró que mantiene “una separación interna” entre sus equipos de investigación clínica y aquellos involucrados en procesos de acceso y contratación pública.
La empresa señaló que sus actividades se rigen por “políticas de cumplimiento y estándares éticos internacionales”. También indicó que ha trabajado con cerca de 100 profesionales de la salud en el Perú en ensayos clínicos, bajo supervisión de comités de ética y del Instituto Nacional de Salud.
No aclaró, sin embargo, si tenía conocimiento de que algunos de estos médicos participaban, al mismo tiempo, en la elaboración o aprobación de los documentos técnicos que sustentaron el uso del pembrolizumab en el sistema público.
Cómo el INEN concentró el poder de decisión
La forma en que se aprueban los medicamentos oncológicos de alto costo en el Perú no siempre estuvo concentrada en el INEN. Para entender cómo terminó ganando ese poder de decisión, hay que volver al reglamento de la Ley Nacional del Cáncer aprobado en 2022, que diseñó un sistema con varios filtros técnicos, pero dejó pendientes reglas importantes para que pudiera funcionar plenamente.
Ese reglamento establecía una ruta. El proceso empezaba en los hospitales, donde el médico tratante sustentaba la necesidad del medicamento y el comité farmacoterapéutico evaluaba la solicitud.
Cuando el tratamiento superaba el umbral de 40 mil soles al año —es decir, cuando implicaba un gasto elevado para el sistema de salud— el caso ya no debía resolverse solo en el hospital. Tenía que remitirse a RENETSA, un espacio técnico coordinado por el Instituto Nacional de Salud. Allí, con participación del Instituto de Evaluación de Tecnologías en Salud e Investigación de EsSalud y de la Dirección General de Medicamentos, Insumos y Drogas (Digemid) se evaluaba la evidencia antes de emitir una recomendación.

En la práctica, esto significaba que los tratamientos de alto costo no se aprobaban de inmediato. Había que compararlos con otras opciones disponibles —en un escenario donde no siempre está claro cuál es mejor— y tener en cuenta que su precio podía afectar de manera importante el presupuesto del sistema de salud. Eran decisiones complejas que no debían quedar en manos de una sola instancia.
Pero ese diseño no llegó a ponerse en marcha tal como estaba previsto.
El reglamento definía el procedimiento general, pero requería normas complementarias para poder aplicarse. Como esas disposiciones no se emitieron a tiempo, los hospitales —incluido el INEN— quedaron sin una vía operativa para seguir adquiriendo medicamentos para sus pacientes.
Ante ese vacío, en enero de 2023 el Gobierno aprobó el Decreto Supremo N° 001-2023-SA como una medida transitoria para permitir esas compras mientras se definían las reglas pendientes. La norma autorizó a los hospitales y al INEN a seguir adquiriendo medicamentos de alto costo siempre que las solicitudes fueran evaluadas por sus comités farmacoterapéuticos y se consideraran las evaluaciones de la RENETSA en caso existieran.
Esto significó que la evaluación por parte de RENETSA dejaba de ser un paso necesario antes de la compra y pasaba a ser una referencia posible. Así, el circuito previsto en el reglamento se volvió más flexible y con menos filtros obligatorios.
El cambio decisivo llegó apenas un mes después.
En febrero de 2023, la entonces ministra de Salud, Rosa Gutiérrez, aprobó la Resolución Ministerial N° 191-2023/MINSA que estableció que bastaba con la opinión favorable del Comité Farmacoterapéutico del INEN para sustentar la compra de medicamentos oncológicos de alto costo.
Con ese aval, la Dirección de Prevención y Control del Cáncer podía gestionar estas adquisiciones para todo el sistema a través de la central de compras del Ministerio de Salud.
Así, el proceso dejó de depender de varias instancias técnicas y pasó a concentrarse en una sola institución. El INEN —que antes era parte del circuito— se convirtió en el principal filtro, sin que se establecieran reglas claras para prevenir conflictos de interés entre los médicos que participan en decisiones públicas de salud que involucran millones de soles.
Durante más de un año, el Ministerio de Salud realizó compras bajo este esquema, pero había un problema de fondo: esas decisiones se apoyaban en una resolución ministerial que no podía cambiar lo que establecía un decreto supremo.
Abogados consultados por Salud con lupa coinciden en que el sistema funcionó en una zona gris legal, donde una norma de menor rango terminó definiendo decisiones que comprometían millones de soles del presupuesto público.
Recién en octubre de 2024, bajo la gestión del ministro César Vásquez, el Gobierno emitió el Decreto Supremo N° 018-2024-SA. Con esa norma, lo que hasta entonces había operado en la práctica quedó incorporado en el reglamento: el INEN pasó a ser la principal instancia para aprobar medicamentos oncológicos de alto costo dentro del sistema público.

Este giro normativo respondió a recomendaciones de una comisión especial del Congreso creada para vigilar el gasto en la atención del cáncer, impulsada por el legislador fujimorista Alejandro Aguinaga.
En sus propias palabras, el objetivo era “quitar burocracia” y acelerar las compras. Sin embargo, en ese espacio no se han discutido los conflictos de interés ni los riesgos de concentrar millones de soles en pocos fármacos, dejando de lado otras necesidades de los pacientes con cáncer.
Más presupuesto, pero en menos medicamentos
Un informe de Digemid de 2025 muestra un cambio drástico en cómo se está gastando el dinero público en medicamentos contra el cáncer, que coincide con el periodo en que el INEN pasó a concentrar el poder de decisión. Un pequeño grupo de fármacos de alto costo, entre ellos el pembrolizumab, pasó a concentrar la mayor parte del presupuesto, mientras el resto de tratamientos esenciales fue quedando relegado.
Hasta 2022, los medicamentos oncológicos esenciales —los que deben estar disponibles en hospitales públicos y que usan la mayoría de pacientes— concentraban cerca del 90% del gasto estatal. Para 2024, esa proporción cayó al 12,5%.
Es decir, aunque el presupuesto total aumentó de 26,8 millones de soles en 2022 a 181 millones en 2024, cada vez menos dinero se destinó a los tratamientos que forman parte del Petitorio Nacional de Medicamentos Esenciales (PNUME).

Esta tendencia se acentuó aún más en 2025. Un análisis de contratos públicos realizado por Salud con lupa muestra que cinco medicamentos oncológicos de alto costo absorbieron el 91% del presupuesto.
El principal fue el pembrolizumab: el Estado destinó 95 millones de soles en un solo contrato de 14,800 unidades para cubrir la demanda de este año, el monto más alto registrado para un fármaco oncológico en el sistema público. El resto de tratamientos representó apenas el 8,94%.
La magnitud de ese gasto se explica por la duración y el precio del tratamiento con pembrolizumab. En cánceres como el de pulmón o cuello uterino, se administran dos viales cada tres semanas y hasta por un año. En promedio, cada paciente requiere alrededor de 34 viales.
Esto hace que, pese al aumento del presupuesto, el sistema solo pueda cubrir la terapia para un número limitado de personas.
Sin embargo, la demanda de pembrolizumab creció con rapidez, presionando aún más los recursos disponibles.
En octubre de 2023, el INEN reportaba un uso de 38 viales al mes; un año después, el consumo había subido a 328. En 2025, el uso mensual era de 270 viales, aunque el propio instituto solicitó incrementarlo. En abril de ese año, informó que atendía a 135 pacientes y proyectaba llegar a 151 hacia fin de año.
Este aumento ya generaba tensiones dentro del sistema de salud. Documentos revisados por Salud con lupa, obtenidos por la Ley de Transparencia, muestran un intercambio de oficios entre el gerente general del INEN, Yván Palomino, y la entonces directora de Prevención y Control del Cáncer del Ministerio de Salud, Essy Maradiegue, la instancia encargada de asignar el presupuesto oncológico.
Mientras el INEN buscaba ampliar las compras del medicamento, el Ministerio sostenía que había stock suficiente y advirtió que no se incrementaría la adquisición sin contar antes con herramientas para monitorear el uso de medicamentos de alto costo.
Hay otro dato clave. En sus primeros contratos, el Estado peruano pagó hasta 30% más que Argentina y Chile por el pembrolizumab. En 2023, en su primera compra pagó 8,752 soles por vial; en 2025, el precio bajó a 6,450 soles. Pero esa reducción no volvió accesible el tratamiento. Y eso que Perú exonera del IGV y de los derechos arancelarios a los medicamentos oncológicos importados desde hace más de una década.
“Cuando el precio del fármaco sigue siendo alto y, además, hay un único proveedor, quitar impuestos no es suficiente. Puede reducirse el precio, pero el tratamiento sigue siendo demasiado caro para cubrir a más pacientes”, explicó Javier Llamoza, de Acción Internacional para la Salud e investigador de la industria farmacéutica en Perú.
La crisis que viven los pacientes
Mientras se toman decisiones millonarias y cambian las reglas de compra, los pacientes enfrentan interrupciones y retrasos en sus tratamientos. En 2025 y en lo que va de este año, incluso fármacos oncológicos esenciales han dejado de estar disponibles en decenas de hospitales del país.
En el INEN y en los institutos regionales oncológicos, varias quimioterapias se detuvieron por la escasez de fármacos como cisplatino, ciclofosfamida e ifosfamida. “Nos dijeron que esperáramos, pero no nos daban una fecha clara para retomarlas. Pasaron semanas hasta que me llamaron”, contó a Salud con lupa un paciente que tuvo que suspender su tratamiento en octubre pasado.
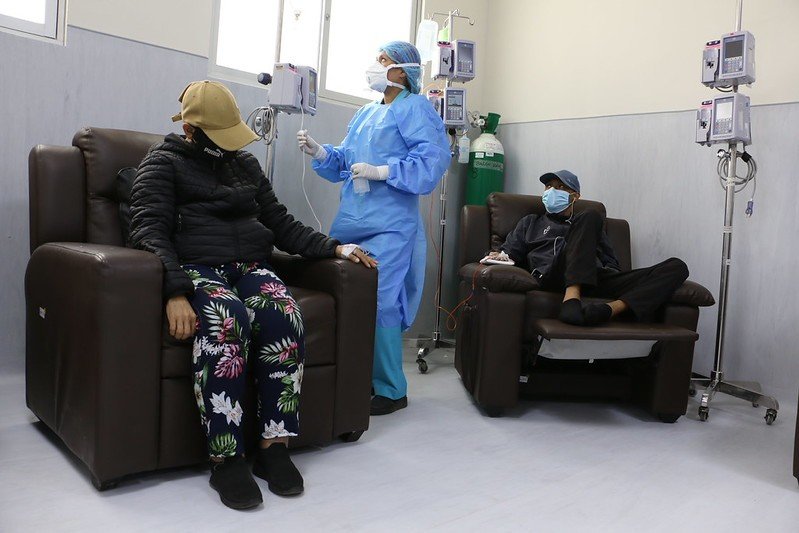
Pese a este escenario, la comisión especial del Congreso que supervisa el gasto en la atención del cáncer ha tenido escasos pronunciamientos sobre el desabastecimiento de medicamentos esenciales. En cambio, ha centrado su atención en la adquisición de fármacos de alto costo.
En un informe de enero de 2026, dirigido al entonces ministro de Salud, Luis Quiroz, la comisión presidida por la congresista Mery Infantes analizó la situación de medicamentos oncológicos aprobados por el Comité Farmacoterapéutico del INEN que luego recibieron una recomendación no favorable de RENETSA.
Aunque en la práctica el INEN había asumido un rol central en la aprobación de estos tratamientos, las evaluaciones de RENETSA —la instancia técnica que analiza su costo y beneficio— seguían emitiéndose y, en algunos casos, cuestionaban esas decisiones.
Según el documento, esto ha impedido que la compra de ciertos medicamentos de alto costo se concrete, lo que ha llevado a la suspensión de tratamientos en pacientes que ya los venían recibiendo y ha generado barreras para nuevos casos. Frente a ello, la comisión propuso “modificar el proceso de evaluación y revisar las decisiones de RENETSA”.
Esta postura también aparece en las intervenciones de organizaciones de pacientes convocadas por la comisión y coincide con críticas planteadas por médicos del INEN y representantes de la Asociación de Laboratorios Farmacéuticos del Perú (ALAFARPE), el gremio que agrupa a compañías multinacionales que operan en el país y del que forma parte Merck Sharp & Dohme.
Dos meses después, en marzo de 2026, el foco se trasladó a las compras. En un nuevo informe dirigido al ministro de Salud, Juan Carlos Velasco, la comisión pidió “programar con urgencia siete medicamentos oncológicos de alto costo que aún no habían sido incluidos en la compra centralizada”.
El documento también exigió autorizar su adquisición sin esperar el resultado completo de la evaluación técnica.
Aunque en ese mismo informe la comisión advirtió que existían 32 productos oncológicos y de diagnóstico en riesgo de desabastecimiento o quiebre de stock durante 2026 —entre ellos varios tratamientos esenciales—, el énfasis de sus recomendaciones estuvo puesto en acelerar la compra de medicamentos de alto costo.

La Dirección de Prevención y Control del Cáncer, encargada de conducir la política oncológica y definir el uso del presupuesto, también ha sido criticada por la propia comisión en este proceso. Pese a ello, no ha asumido una posición clara ni firme.
Su directora ejecutiva, Essy Maradiegue, no respondió durante semanas a las consultas de Salud con lupa. El 25 de abril pasado fue reemplazada en el cargo por Víctor Palacios Cabrejos, asesor de la comisión del Congreso que impulsaba esos cuestionamientos y que, además, mantiene vínculos no transparentados con la industria farmacéutica.
El Colegio Médico y los conflictos de interés
Durante esta investigación, Salud con lupa pidió al Colegio Médico del Perú su postura sobre el papel de médicos vinculados a la industria farmacéutica en decisiones sobre la aprobación y financiamiento de medicamentos de alto costo en el sistema público. En los casos documentados en este reportaje, su Comité de Medicamentos advirtió una preocupación clara.
“Cuando un médico participa en decisiones que involucran el uso de recursos públicos —como la aprobación de medicamentos de alto costo— su rol deja de ser exclusivamente clínico y pasa a tener una dimensión de salud pública y gestión de recursos. En ese contexto, los estándares éticos deben ser más estrictos, ya que las decisiones no afectan solo a un paciente, sino a toda la población y al sistema de salud en su conjunto”, señaló en una respuesta escrita.
En esa línea, el Comité advirtió que la participación de médicos que han sido investigadores clínicos de un mismo medicamento —como el pembrolizumab, de Merck Sharp & Dohme— en decisiones sobre su aprobación o financiamiento público representa un riesgo claro de conflicto de interés.
“Aunque la participación en investigación clínica es legítima, cuando existe un vínculo directo con un producto evaluado en decisiones públicas, se requiere una gestión más estricta. La participación en comités de decisión cuando existe financiamiento o vínculo con la industria constituye un conflicto de interés; en estos casos, el médico debe abstenerse de dichas funciones”, apuntó.
El Código de Ética del Colegio Médico del Perú establece que la salud del paciente debe prevalecer sobre intereses del mercado o de la investigación y exige que los médicos actúen con independencia frente a la industria farmacéutica. También advierte que la aceptación de incentivos económicos puede sesgar decisiones sobre prescripción, inclusión en petitorios o compras públicas.
Por ello, obliga a declarar los conflictos de interés y, cuando corresponde, a abstenerse de participar. Incluso prohíbe que médicos con financiamiento o remuneración de empresas relacionadas integren comités farmacológicos o participen en procesos de adquisición.

Frente a este problema, el Comité señaló que el país necesita fortalecer tres dimensiones: normas más específicas que definan claramente qué constituye un conflicto de interés, mecanismos de supervisión efectivos que aseguren su cumplimiento y medidas proporcionales que incluyan sanciones cuando corresponda.
“Más allá de lo individual, estos casos evidencian la necesidad de mejorar los sistemas de control institucional. El Colegio Médico puede evaluar posibles infracciones al Código de Ética, incluso de oficio. Sin embargo, más allá de la sanción, estos casos deben servir para fortalecer los mecanismos de prevención y regulación”, concluyó.
Mientras tanto, el Ministerio de Salud se ha negado a responder a todas las solicitudes de entrevista enviadas desde febrero, pese al impacto de estas decisiones en los pacientes.
Una directiva para ordenar decisiones bajo presión
En octubre de 2025, el Instituto Nacional de Salud aprobó una directiva orientada a evitar que la incorporación de medicamentos de alto costo dependa de decisiones aisladas o influenciadas por intereses particulares.
La norma establece que estas decisiones deben evaluarse en tres dimensiones: la eficacia y seguridad del medicamento, su sostenibilidad para el sistema y su impacto en el acceso, es decir, si su uso permite beneficiar a quienes lo necesitan sin desplazar recursos de otros pacientes.
Además, incorpora reglas más estrictas: obliga a declarar conflictos de interés, exige sustento en evidencia científica más robusta e incluye la participación de pacientes en el proceso de evaluación.
Sin embargo, su implementación ha abierto un nuevo frente de conflicto. Desde el Congreso, la comisión especial ha exigido al Ministerio de Salud no aplicar este sistema de evaluación y reemplazarlo por un mecanismo distinto.